8. 治療の選択肢
2026.04.03
消化管再生の三原則:進化医学と栄養療法による根治へのアプローチ
消化管に関連する疾患の基本的な治療方針は、主に以下の3つの原則に基づいています。
すなわち、
① 人類の進化の過程で消化管が適応してきた自然な食物に立ち返ること、
② 食物アレルギーや不耐性を引き起こす食品を避けること、
③ そして、必要に応じて最適量の栄養素を補うことです[1]。

こうした原則を踏まえ、病気の予防のためには「生きている食物」、すなわち加熱や加工が最小限に抑えられた自然食品を常食することが重要です。
たとえ病気がすでに発症していたとしても、完全な治癒が望めないケースであっても、以下のような食事指針に基づいた改善は、症状の進行を抑えたり、治癒プロセスを促進する助けになると考えられています。
自然な食材の選択:できるだけ自然に近い、丸ごとの食材を選ぶこと。加工食品やジャンクフードは避けるべきです。
アレルゲンの排除:アレルギー反応や過敏症を引き起こす食品(例:グルテン、乳製品、大豆など)は摂取を避けること。
⑴ サプリメントの使用が必要な理由
こうした食事改善に加え、栄養補助食品(サプリメント)を併用する意義は、主に2点あります。
第一に、消化管に炎症や機能低下がある場合、食事からの栄養素吸収効率が大幅に低下している可能性があります。
特に加工食品を中心とした現代の食生活では、ビタミンやミネラルの含有量が極めて少なく、慢性的な微量栄養素欠乏が起こりやすくなっています[2・3]。
第二に、病気からの回復に際しては、通常よりも多くの栄養素が必要とされるため、治療的な意味を持つ“高用量”の栄養素投与(オーソモレキュラー療法)が有効です[4]。

⑵ 粘膜修復と免疫調整のための重要栄養素
たとえば、水溶性のビタミンB群は消耗が早く、代謝ストレス下では不足しやすいため、50〜100mgのビタミンB群を含む高用量マルチビタミン剤の使用が推奨されます。
これは市販でも容易に入手可能です[5]。
また、アスコルビン酸(ビタミンC)を高用量で摂取することにより、便を軟化させて便秘を改善し、同時に傷ついた粘膜組織の修復も促進されることが知られています[6]。
ビタミンCの便通調整効果は、安全な上に用量依存的であるため、摂取量を調節することで個人に適した量を見出すことが可能です。
脂溶性ビタミンであるビタミンEも、800〜4000 IUの範囲で投与されることで抗酸化・抗炎症作用を発揮し、クローン病などの難治性消化管疾患において改善が報告されている例もあります[7]。
さらに、マルチミネラル製剤の併用により、亜鉛やマンガンなどの微量元素を補うことも重要です。
これらのミネラルは、消化管の修復や免疫調節に関与しており、不足すると治癒が遅れる可能性があります[8]。

【最新の知見:腸管バリア機能とビタミンD・グルタミンの役割】
近年の研究では、消化管疾患の背後に「腸管壁浸透性の亢進(リーキーガット症候群)」が強く関与していることが明らかになっています[10]。
このバリア機能を修復するために、現在以下の栄養素が特に注目されています。
ビタミンD3:粘膜の「タイトジャンクション(細胞同士の結合)」を強化し、過剰な炎症を抑制する免疫調節因子として不可欠です。血中濃度を最適化(50〜80 ng/mL)することで、IBD(炎症性腸疾患)の再発率低下が報告されています[11]。
L – グルタミン:小腸粘膜細胞の主要なエネルギー源であり、炎症で傷ついた絨毛の再生を強力にサポートします[12]。
ポストバイオティクス(短鎖脂肪酸):食物繊維だけでなく、酪酸などの代謝産物を直接あるいはプレバイオティクス経由で補うことで、大腸粘膜のエネルギー代謝を正常化させます[13]。
⑶ 統合的アプローチの重要性
ただし、強い炎症や感染を伴う病態においては、現代医学的な治療、すなわち鎮痛剤、抗炎症薬、抗菌薬などの使用も並行して検討すべきです。
病変が不可逆的に進行している場合には、外科的治療が必要となることもあります。
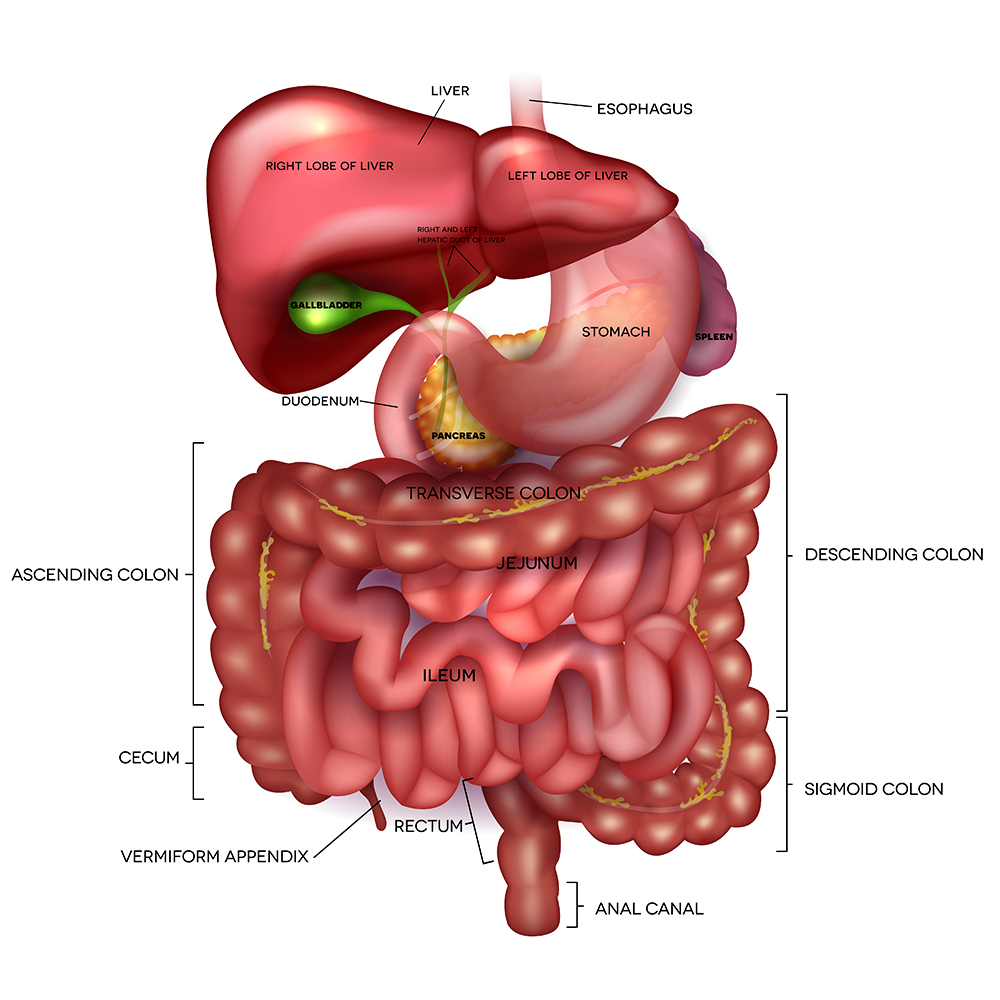
また、消化管の中でも、回腸末端や直腸などの解剖学的・機能的に特殊な部位では、治療反応性が異なるため、追加的な治療やサプリメント調整が必要となる場合があります[9]。
次回は「口とのど:口腔・咽頭における栄養療法の役割」をお送りします。

References
Eaton, S. B., & Konner, M. (1985). Paleolithic nutrition. New England Journal of Medicine.
Davis, D. R. (2009). Declining fruit and vegetable nutrient composition. HortScience.
Ames, B. N. (2006). Low micronutrient intake may accelerate the degenerative diseases of aging through allocation of scarce micronutrients by triage. PNAS.
Hoffer, A., & Saul, A. W. (2008). Orthomolecular Medicine Explained. Basic Health Publications.
Kennedy, D. O. (2016). B Vitamins and the Brain. Nutrients.
Cathcart, R. F. (1981). Vitamin C, titrating to bowel tolerance, anascorbemia, and acute induced scurvy. Medical Hypotheses.
Belluzzi, A., et al. (1996). Effects of new fish oil derivative on relapse in Crohn’s disease. New England Journal of Medicine. (Related to lipid-soluble antioxidants)
Skrovanek, S., et al. (2014). Zinc and gastrointestinal disease. World Journal of Gastrointestinal Pathophysiology.
Goke, M., et al. (1996). Differential effects of mucosal growth factors on small intestinal and colonic epithelial cells. Digestive Diseases and Sciences.
Fasano, A. (2020). All disease begins in the (leaky) gut: role of zonulin-mediated gut permeability in the pathogenesis of some chronic inflammatory diseases. F1000Research.
Gubatan, J., et al. (2019). Vitamin D in Inflammatory Bowel Disease: More than Just Bone Health. Current Opinion in Gastroenterology.
Kim, M. H., & Kim, H. (2017). The Roles of Glutamine in the Intestine and Its Implication in Intestinal Diseases. International Journal of Molecular Sciences.
Liu, H., et al. (2025). Postbiotics: The frontier of gut microbiome-derived therapies in gastrointestinal repair. Trends in Endocrinology & Metabolism.
